3. Aldehid/Alkanal
a. Rumus umum aldehid
Aldehid atau alkanal dapat dianggap sebagai turunan alkana dengan mengganti 1 atom H dari alkana dengan gugus fungsi
senyawa aldehid mempunyai rumus umum:
Pada aldehid gugus fungsi terletak di ujung rantai C.
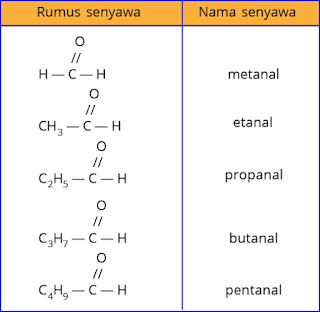
Contoh beberapa senyawa aldehid
b. Tata nama aldehid
Nama IUPAC
Nama IUPAC untuk aldehid adalah alkanal. Untuk alkanal yang mempunyai isomer pemberian namanya sebagai berikut:
Rantai pokok adalah rantai terpanjang yang mengandung gugus fungsi -COH.
Nama aldehid sesuai nama rantai pokok, diberi akhiran al.
Penomoran dimulai dari gugus fungsi. Pemberian nama dimulai dengan nama cabang-cabang yang disusun menurut abjad, kemudian nama rantai pokok. Posisi gugus fungsi tidak perlu disebutkan karena selalu pada atom C nomor satu.
Contoh:
Nama trivial
Nama trivial dari aldehid menggunakan akhiran aldehid.
Contoh:
c. Isomer aldehid
Aldehid tidak mempunyai isomer posisi karena gugus fungsi dari aldehid terletak di ujung rantai C. Isomer pada aldehid terjadi karena adanya cabang dan letak cabang, jadi merupakan isomer struktur. Isomer aldehid mulai terdapat pada suku ke-4 yaitu butanal.
Contoh :
isomer struktur butanal (C4H8O)
Isomer struktur pentanal
d. Sifat-Sifat Aldehid
Sifat Fisis
Suku pertama aldehid pada suhu kamar berwujud gas yang berbau merangsang, sedangkan suku berikutnya berwujud cair yang berbau harum dengan semakin panjang rantai karbonnya.
Sifat Kimia
1) Bila direduksi (ditambah H2) menghasilkan alkohol primer
2) Dapat mengadisi HCN
3) Bila dioksidasi menghasilkan asam karboksilat.
4) Dapat mereduksi larutan fehling membentuk endapan merah
Pereaksi Fehling adalah campuran CuSO4(aq) dengan kalium natrium tartrat dalam suasana basa. Pereaksi Fehling dapat dianggap CuO. Reaksi aldehid dengan larutan Fehling menghasilkan endapan merah bata dari Cu2O.
5) Dapat mereduksi pereaksi tollens membentuk endapan perak (Ag).
Pereaksi Tollens adalah larutan AgNO3 dalam larutan NH3 berlebih. Pereaksi Tollens dapat dianggap sebagai larutan Ag2O. Reaksi aldehid dengan larutan Tollens akan menghasilkan endapan perak. Endapan perak yang dihasilkan akan melapisi tabung membentuk cermin. Oleh karena itu, reaksi ini disebut reaksi cermin perak.
e. Pembuatan Aldehid
Aldehid dapat dibuat dari oksidasi alkohol primer. Oksidasi yang digunakan adalah KMnO4 atau K2Cr2O7.
Contoh:
Secara komersial, formaldehid dibuat dengan mereaksikan uap alkohol (metanol) dengan katalis tembaga dan dipanaskan.
f. Kegunaan Aldehid
a) Larutan 37% formaldehid (metanal) dalam air disebut formalindigunakan untuk mengawetkan benda-benda anatomi.
b) Formaldehid untuk membuat damar buatan, plastik, dan insektisida.
c) Etanol sebagai bahan karet dan damar buatan serta zat warna.
4. Keton/Alkanon
a. Rumus umum keton
Alkanon merupakan isomer fungsi dari aldehid dengan gugus fungsional
Rumus umum alkanon adalah
Berikut contoh senyawa alkanon
b. Tata nama keton
Nama IUPAC
Nama IUPAC dari keton adalah alkanon. Suku terendah dari alkanon adalah propanon. Untuk alkanon yang mempunyai isomer pemberian nama senyawa sebagai berikut
1) Rantai pokok adalah rantai terpanjang yang mengandung gugus fungsi diberi nama
alkanon.
2) Penomoran dimulai dari C ujung yang terdekat dengan posisi gugus fungsi sehingga C yang mengandung gugus fungsi mendapat nomor terkecil.
3) Pemberian nama sama seperti alkanol. Cabang-cabang disebut lebih dulu, disusun menurut abjad dan diberi awalan yang menyatakan jumlah cabang tersebut. Letak gugus fungsi dinyatakan dengan awalan angka pada nama rantai pokok.
Contoh:
Nama lazim
Nama lazim keton adalah alkil-alkil keton. Jika gugus alkil sama disebut dialkil keton.
Contoh:
c. Isomer keton
Isomer posisi senyawa keton
Keton mempunyai isomer posisi, karena letak gugus fungsi dapat berbeda. Isomer posisi mulai terdapat pada pentanon.
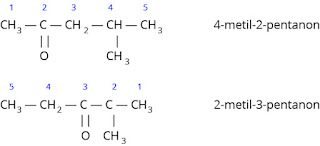
Contoh:
Isomer C5H10O
Isomer fungsi antara aldehid dan keton
Aldehid dan keton mempunyai rumus molekul sama tetapi gugus fungsinya berbeda.
Rumus molekul untuk aldehid dan keton adalah
Contoh:
d. Sifat-Sifat Alkanon
Sifat Fisis
Alkanon suku rendah pada suhu kamar berwujud cair tidak berwarna, berbau harum, dan mudah larut dalam air. Suhu yang lebih tinggi sukar larut dalam air, sedangkan alkanon suku tinggi berwujud padat.
Sifat Kimia
1) Dapat direduksi (ditambah H2) menjadi alkohol sekunder
2) Dapat mengadisi HCN :
3) Tidak dapat mereduksi larutan fehling dan tollens (sehingga dapat digunakan untuk membedakan aldehid dengan alkanon).
e. Reaksi membedakan aldehid dan keton
Aldehid dan keton dapat dibedakan dengan cara mereaksikan senyawa-senyawa itu dengan oksidator seperti pereaksi Fehling dan pereaksi Tollens. Aldehid bereaksi positif dengan kedua pereaksi itu, dengan Fehling menghasilkan endapan merah bata, dengan Tollens menghasilkan cermin perak. Sedangkan keton tidak dapat dioksidasi, berarti reaksi negatif.
Aldehid + Fehling → endapan merah bata
Aldehid + Tollens → cermin perak
Keton + Fehling tidak bereaksi
Keton + Tollens tidak bereaksi
f. Pembuatan Alkanon
Alkanon dapat dibuat melalui beberapa cara, diantaranya sebagai berikut:
- Dengan mengoksidasi alkohol sekunder.
- Dengan distilasi kering garam-garam alkali atau alkali tanah karboksilat
g. Kegunaan keton
Senyawa keton yang paling dikenal dalam kehidupan sehari-hari adalah aseton (propanon). Kegunaan aseton yaitu sebagai berikut.
1) Pelarut senyawa karbon, misalnya untuk membersihkan cat kuku (kutek), melarutkan lilin, dan plastik.
2) Untuk membuat kloroform (obat bius), iodoform, dan isopren.
kloroform dibuat dengan mereaksikan aseton dengan gas klor dan NaOH.




























Tidak ada komentar:
Posting Komentar